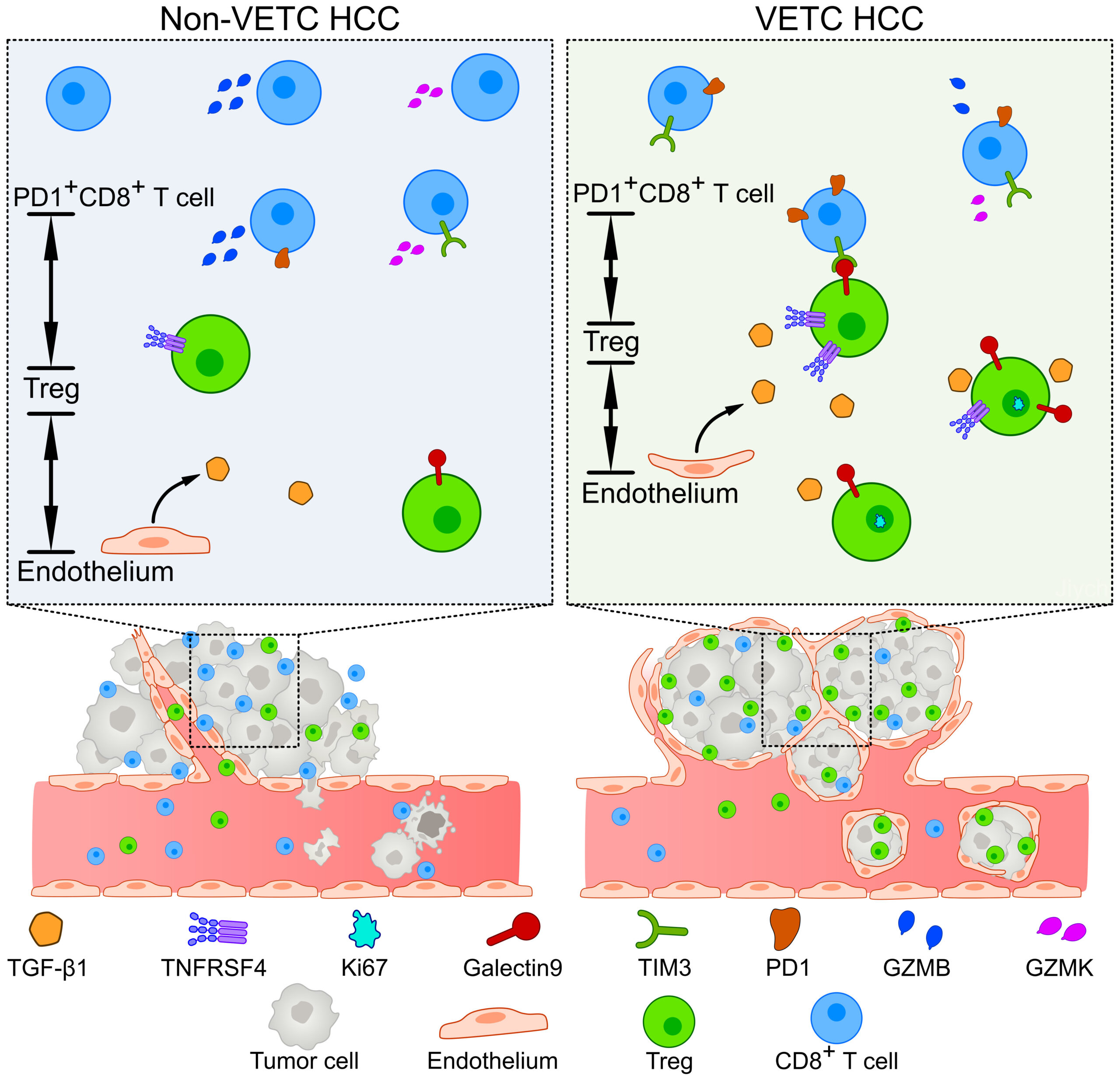
包覆肿瘤簇的血管(VETC)是肝细胞癌(HCC)中独特的血管模式,促进整个肿瘤簇的非侵入性转移。VETC与肿瘤微环境之间的相互作用需要进一步探讨。我们发现,与人类非VETC-HCCs相比,VETC肿瘤表现出更多的PD1+CD8+ T细胞和Tregs,尤其是TNFRSF4+ Tregs和Ki67+ Tregs,这些细胞表现出增强的免疫抑制和增殖活性。这种免疫抑制状态也在VETC-HCCs肿瘤栓塞中检测到,栓塞中的Treg密度与转移性细胞增殖呈正相关。VETC-HCCs显示TNFRSF4+ Tregs/Ki67+ Tregs与PD1+CD8+ T细胞之间存在丰度相关性、更接近的空间接近性以及更强的免疫抑制配体-受体相互作用。耗尽小鼠Tregs减少了原发病灶中的PD1+CD8+ T细胞,肿瘤栓塞和VETC-异体移植物转移灶,并减弱了异体移植物转移。VETC-HCCs内皮细胞中TGF-β1水平上调,并与TNFRSF4+ Tregs/Ki67+ Tregs富集相关。破坏VET形成降低了内皮的TGF-β1表达,降低了TNFRSF4+ Tregs、Ki67+ Tregs、PD1+CD8+ T细胞和T/CD8+ T细胞比值。总体而言,VETC可能通过TGF-β1增强Treg活性,而Tregs通过免疫抑制配体-受体相互作用促进并维持CD8+ T细胞的枯竭,从而塑造免疫抑制微环境,使肿瘤群群保留该生态位以扩散。这些发现揭示了肿瘤免疫微环境形成的机制,并为精准医疗提供了基础。
关键词: 肝病学;免疫学;肝癌;Tregs;血管生物学。